Belajar Pintar Materi SMP, SMA, SMK
BelajarPintarV3
Kimia
Laju Reaksi
MATERI
Pengertian Laju Reaksi

Laju Reaksi adalah laju berkurangnya jumlah pereaksi untuk satuan waktu atau bertambahnya jumlah hasil reaksi untuk setiap satuan waktu.
Ukuran jumlah zat dalam reaksi kimia umumnya dinyatakan sebagai konsentrasi molar atau molaritas (M), dengan demikian maka laju reaksi menyatakan berkurangnya konsentrasi pereaksi atau bertambahnya konsentrasi zat hasil reaksi setiap satu satuan waktu (detik). Satuan laju reaksi dinyatakan dalam satuan mol dm-3 det-1 atau mol/liter detik.
Stoikiometri laju reaksi
Secara umum untuk reaksi yang dinyatakan dengan persamaan reaksi :
aA + bB ---> cC + dD
Berlaku :
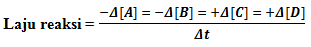
Jika dalam grafik, laju reaksi digambarkan sebagai berikut:
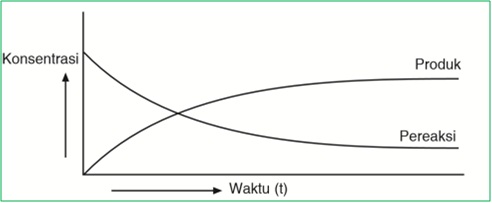
Penentuan Laju Reaksi

Penentuan laju reaksi dapat dilakukan dengan cara fisika atau cara kimia. Dengan cara fisika yaitu berdasarkan sifat-sifat fisis campuran yang dipengaruhi oleh konsentrasi campuran, misalnya daya hantar listrik, tekanan (untuk reaksi gas), adopsi cahaya dll.
Sedangkan dengan cara kimia yaitu dengan menghentikan reaksi secara tiba-tiba setelah selang waktu tertentu, kemudian konsentrasinya ditentukan dengan metode analisis kimia.
1.
Jawablah soal berikut ini!
Berkurangnya jumlah pereaksi untuk satuan waktu atau bertambahnya jumlah hasil reaksi untuk setiap satuan waktu disebut...
A. Laju Reaksi
B. Hukum Laju Reaksi
C. Entalpi
D. Hukum Kekekalan Energi
E. Hukum Termokimia
JAWABAN BENAR
A.
Laju Reaksi
PEMBAHASAN
Laju reaksi adalah berkurangnya jumlah pereaksi untuk satuan waktu atau bertambahnya jumlah hasil reaksi untuk setiap satuan waktu.
2.
Jawablah soal berikut ini!
Penentuan laju reaksi dapat dilakukan dengan cara...
A. Biologi atau Kimia
B. Fisika atau Kimia
C. Biologi atau Fisika
D. Entalpi
E. Gravitasi
JAWABAN BENAR
B.
Fisika atau Kimia
PEMBAHASAN
Penentuan laju reaksi dapat dilakukan dengan cara fisika atau cara kimia.
3.
Jawablah soal berikut ini!
Sebanyak 0,5 mol gas NO2 dipanaskan dalam ruangan dengan volume 5 liter sehingga membentuk dinitrogen pentaoksida menurut persamaan:
4NO2(g) + O2(g) --> 4N2O5(g)
Dalam 20 detik pertama terbentuk 0,5 mol N2O5. Laju pengurangan NO2 adalah....
A. 5 x 10-2
B. 5 x 10-4
C. 5 x 103
D. 5 x 10-3
E. 5 x 10-1
JAWABAN BENAR
D.
5 x 10-3
PEMBAHASAN

4.
Jawablah soal berikut ini!
Dari reaksi 2N2O5 --> 4NO2 + O2 diperoleh data pembentukan senyawa NO2 sebagai berikut:
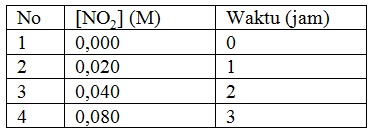
Laju pembentukan NO2 adalah....
A. 5,5 x 10-3 M/s
B. 5,5 x 10-4 M/s
C. 5,5 x 10-5 M/s
D. 5,5 x 10-6 M/s
E. 5,5 x 10-7 M/s
JAWABAN BENAR
D.
5,5 x 10-6 M/s
PEMBAHASAN
Perhatikan data no. 2 dan 3
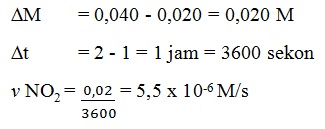
5.
Jawablah soal berikut ini!
Laju reaksi A + B --> AB dapat dinyatakan sebagai….
A. penambahan konsentrasi A tiap satuan waktu
B. penambahan konsentrasi B tiap satuan waktu
C. penambahan konsentrasi AB tiap satuan waktu
D. penambahan konsentrasi A dan B tiap satuan waktu
E. penambahan konsentrasi A, B dan AB tiap satuan waktu
JAWABAN BENAR
C.
penambahan konsentrasi AB tiap satuan waktu
PEMBAHASAN
Karena A dan B merupakan reaktan sehingga akan mengalami pengurangan tiap satuan waktu. Sedangkan AB merupakan produk dari reaktan sehingga akan terus bertambah tiap satuan waktu.
6.
Jawablah soal berikut ini!
Dalam suatu praktikum kimia, seorang siswa memasukkan 8 g zat A (Ar A = 65) ke dalam tabung reaksi yang berisi 200 mL larutan HCl 2 M. Setelah reaksi berlangsung selama 2 menit, zat A masih tersisa sebanyak 1,5 g. Berapakah laju pengurangan zat A….
A. 3,2 x 10-2 M s-1
B. 3,2 x 10-3 M s-1
C. 3,2 x 10-4 M s-1
D. 4,2 x 10-2 M s-1
E. 4,2 x 10-3 M s-1
JAWABAN BENAR
E.
4,2 x 10-3 M s-1
PEMBAHASAN


Oops!!!
Yah, jawaban kamu meleset nih. Ingin melihat pembahasan soal ini?

BENAR!!!
Selamat!
Jawaban kamu benar. Ingin lihat pembahasan soal ini?
footer_v3
Bersama Aku Pintar temukan jurusan kuliah yang tepat
sesuai minat dan bakatmu.
Aku Pintar memiliki visi membuat pendidikan merata, mudah dijangkau, dan terjangkau dengan Program Journey Pintar yang merupakan sebuah program persiapan lengkap bagi siswa SMA/SMK/sederajat yang ingin masuk ke perguruan tinggi impiannya.
Kontak Kami
Grand Slipi Tower Lt. 42
Jl. S. Parman Kav 22-24
Jakarta Barat
© 2024 Aku Pintar. All Rights Reserved

