Belajar Pintar Materi SMP, SMA, SMK
BelajarPintarV3
Kimia
Reaksi Reduksi Oksidasi dan Tata Nama Senyawa
MATERI
Tata Nama Senyawa Ion

Senyawa ion terdiri dari kation (ion positif) dan anion (ion negatif). Pada umumnya, kation merupakan ion logam dan anion merupakan ion nonlogam.
Kation
- Kation dari unsur logam diberi nama sama dengan unsur logam tersebut.
Contoh:
Ion natrium (Na+), ion kalsium (Ca2+), ion perak (Ag+) - Jika logam dapat membentuk kation dengan muatan berbeda, jumlah muatannya ditulis dengan angka Romawi dalam tanda kurung setelah nama unsur logam itu.
Contoh:
Ion besi(II) (Fe2+), ion besi(III) (Fe3+) - Kation dari unsur nonlogam umumnya memiliki akhiran -ium.
Contoh:
Ion amonium (NH4+), ion hidronium (H3O+)
Berikut merupakan nama-nama kation:
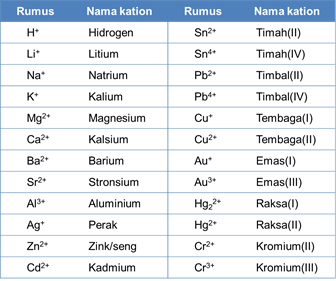
Anion
- Anion monoatom diberi nama dengan akhiran -ida pada nama unsur tersebut.
Contoh:
Ion hidrida (H-), ion oksida (O2-), ion nitrida (N3-), ion fluorida (F-) - Anion poliatom yang mengandung unsur oksigen (oksoanion) diberi nama dengan akhiran -at ataupun -it. Akhiran -at digunakan untuk anion poliatom yang memiliki atom O lebih banyak dibanding anion dengan akhiran -it.
Contoh:
Ion nitrat (NO3-), ion nitrit (NO2-). ion sulfat (SO42-), ion sulfit (SO32-) - Anion yang diturunkan dari penambahan H+ pada oksoanion diberi nama dengan menambahkan awalan hidrogen atau dihidrogen.
Contoh:
Ion hidrogen karbonat (HCO3-), ion dihidrogen fosfat (H2PO4-)
Berikut merupakan nama-nama anion:
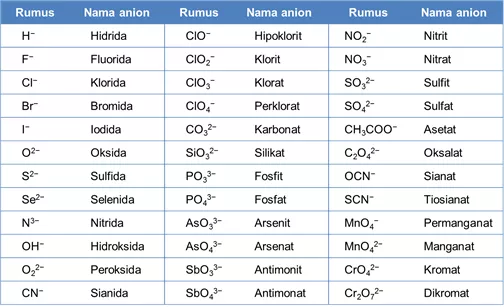
Nama senyawa ion terdiri dari nama kation di awal kemudian diikuti dengan nama anion di akhir.
Contoh :
- KBr : kalium bromida
- BaCl2 : barium klorida
- Ag2S : perak sulfida
- Al(NO3)3 : aluminium nitrat
- FeS : besi(II) sulfida
- Fe2O3 : besi(III) oksida
- CuSO4 : tembaga(II) sulfat
- NH4CN : amonium sianida
Tata Nama Senyawa Kovalen Biner

Senyawa kovalen biner terdiri unsur-unsur nonlogam. Pada bagian ini, tata nama senyawa molekul yang akan dibahas hanya untuk senyawa molekul biner, yaitu senyawa molekul yang hanya terdiri dari dua jenis unsur.
Berikut aturan penamaan senyawa kovalen biner:
- Penulisan unsur pada senyawa kovalen biner diurutkan berdasarkan urutan tertentu.
B – Si – C – Sb – As – P – N – H – S – I – Br – Cl – O – F
Contoh:
H2O bukan OH2,
NH3 bukan H3N. - Penulisan nama kedua ditambahkan -ida dibelakangnya, dan nama unsur depan dan belakang diberi angka indeks.
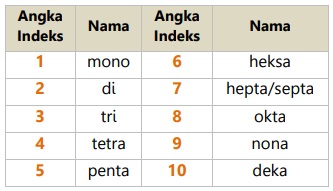
Penulisan angka indeks 1 tidak dipakai pada nama depan, dan tidak wajib pada nama belakang.
Contoh:
CO (karbon monoksida),
NO (nitrogen oksida),
CO2 (karbon dioksida),
N2O3 (dinitrogen trioksida),
NO5 (nitrogen pentaoksida).
Tata Nama Senyawa Asam

Berdasarkan definisi asam basa oleh Arrhenius, senyawa asam adalah senyawa yang bila dilarutkan dalam air akan melepas ion H+. Pada umumnya, asam dapat terionisasi dalam air menjadi ion H+ dan anion yang disebut sisa asam. Penamaan senyawa asam dimulai dari kata ‘asam’ diikuti dengan nama anion sisa asam.
Contoh:
- HCl : asam klorida
- HF : asam fluorida
- H2S : asam sulfida
- HCN : asam sianida
- H2CO3 : asam karbonat
- H2SO4 : asam sulfat
- HClO4 : asam perklorat
Tata Nama Senyawa Organik

Tata nama senyawa organik adalah tata nama senyawa karbon dengan sifat tertentu, dan ditulis dengan nama lazim.
(akan dipelajari lebih lanjut di materi kelas 11 dan 12)
Beberapa contoh senyawa organik adalah sebagai berikut:
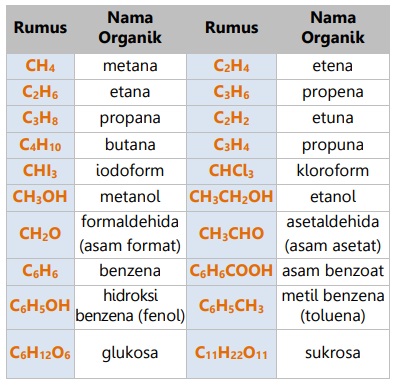
Persamaan Reaksi

Persamaan reaksi menunjukkan perubahan jenis jumlah atom yang bereaksi, dan hasil reaksinya. Persamaan reaksi digunakan untuk mempersingkat penulisan bahasa sehari-hari untuk menjelaskan proses reaksi kimia.
pereaksi/reaktan --> hasil/produk
Ketentuan persamaan reaksi:
- Jumlah atom-atom reaktan dan produk harus sama dan tidak boleh ada satu atom pun yang hilang.
- Setelah rumus unsur/senyawa reaktan atau produk, ditulis wujud zat sewaktu reaksi.
Jika berwujud padat ditulis (s) atau solid.
Jika berwujud cair ditulis (l) atau liquid.
Jika berwujud gas ditulis (g) atau gas.
Jika berbentuk larutan ditulis (aq) atau aqueous.
Contoh:
Logam natrium bereaksi dengan air membentuk larutan natrium hidroksida dan gas hidrogen.
Na(s) + H2O(l) --> NaOH(aq) + H2(g) - Penyetaraan reaksi adalah menyamakan jumlah atom di kiri dan kanan persamaan reaksi, agar menemukan koefisien reaksi tersebut.
Contoh penyetaraan reaksi
Reaksi berikut belum setara Ca(OH)2(aq) + H3PO4(aq) --> Ca3(PO4)2(aq) + H2O(l)
- Tentukan atom-atom yang belum setara.
Atom Ca belum setara,
Atom P belum setara,
Atom H belum setara,
Atom O belum setara. - Setarakan atom dengan urutan kation, anion, hidrogen, lalu oksigen. Biasanya, oksigen akan otomatis setara setelah seluruh atom setara.
- Selain itu, tetapkan salah satu zat apapun untuk memiliki koefisien tetap, dan yang lain memiliki koefisien sementara untuk mempermudah penyetaraan
Hasil penyetaraan reaksi:
3Ca(OH)2(aq) + 2H3PO4(aq) --> Ca3(PO4)2(aq) + 6H2O(l)
Perbandingan koefisien reaksi 3 : 2 : 1 : 6, dengan total atom:
Atom Ca telah setara (total 3),
Atom P telah setara (total 2),
Atom H telah setara (total 12),
Atom O telah setara (total 14).
1.
Senyawa dengan rumus molekul NaCl memiliki nama senyawa ....
A. klorium natrida
B. natrium klorida
C. natrium klor
D. klorium natrium
E. klorida natrium
JAWABAN BENAR
B.
natrium klorida
PEMBAHASAN
NaCl memiliki nama senyawa Natrium Klorida, berasal dari Na atau natrium sebagai kation dan Cl atau klor sebagai anion dengan penambahan kata -ida.
2.
Senyawa dengan rumus molekul CO2 memiliki nama ....
A. karbon monoksida
B. karbon dioksida
C. karbon trioksida
D. karbon tetraoksida
E. karbon pentaoksida
JAWABAN BENAR
B.
karbon dioksida
PEMBAHASAN
Senyawa CO2 memiliki nama Karbon dioksida, karena jumlah atom oksigennya berjumlah 2.
3.
Senyawa yang memiliki rumus kimia KClO4 diberi nama....
A. Kalium klorida
B. Kalium klorat
C. Kalium hipoklorit
D. Kalium perklorat
E. Kalium klorit
JAWABAN BENAR
D.
Kalium perklorat
PEMBAHASAN
Kalium klorida = KCl
Kalium klorat = KClO3
Kalium hipoklorit = KClO
Kalium perklorat = KClO4
Kalum klorit = KClO2
4.
Rumus kimia senyawa difosforus pentaoksida adalah....
A. 2FO5
B. P2O5
C. F2O5
D. 2P2O5
E. 2PO5
JAWABAN BENAR
B.
P2O5
PEMBAHASAN
Difosforus pentaoksida = P2O5
5.
Persamaan reaksi di bawah ini yang benar adalah....
A. C2H6(g) + 7O2(g) --> 2CO2(g) + 3H2O(g)
B. C3H8(g) + 5O2(g) --> 3CO2(g) + 4H2O(g)
C. C4H8(g) + 8O2(g) --> 4CO2(g) + 4H2O(g)
D. C4H10(g) + 9O2(g) --> 4CO2(g) + 5H2O(g)
E. C5H12(g) + 11O2(g) --> 5CO2(g) + 6H2O(g)
JAWABAN BENAR
B.
C3H8(g) + 5O2(g) --> 3CO2(g) + 4H2O(g)
PEMBAHASAN
Persamaan reaksi yang setara adalah:
C3H8(g) + 5O2(g) --> 3CO2(g) + 4H2O(g)

Oops!!!
Yah, jawaban kamu meleset nih. Ingin melihat pembahasan soal ini?

BENAR!!!
Selamat!
Jawaban kamu benar. Ingin lihat pembahasan soal ini?
footer_v3
Bersama Aku Pintar temukan jurusan kuliah yang tepat
sesuai minat dan bakatmu.
Aku Pintar memiliki visi membuat pendidikan merata, mudah dijangkau, dan terjangkau dengan Program Journey Pintar yang merupakan sebuah program persiapan lengkap bagi siswa SMA/SMK/sederajat yang ingin masuk ke perguruan tinggi impiannya.
Kontak Kami
Grand Slipi Tower Lt. 42
Jl. S. Parman Kav 22-24
Jakarta Barat
© 2024 Aku Pintar. All Rights Reserved

