Belajar Pintar Materi SMP, SMA, SMK
BelajarPintarV3
Kimia
Nanoteknologi & Struktur Atom
MATERI
Mengenal Sistem Periodik Unsur

Tabel periodik unsur yang Kalian kenal saat ini adalah sistem periodik modern atau dikenal dengan sistem periodik bentuk panjang yang dicetuskan oleh Henry G Moseley. Kenaikan nomor atom menjadi dasar penyusunan unsur dalam sistem periodik ini sehingga sifat-sifat unsur dapat ditentukan dari nomor-nomor atomnya
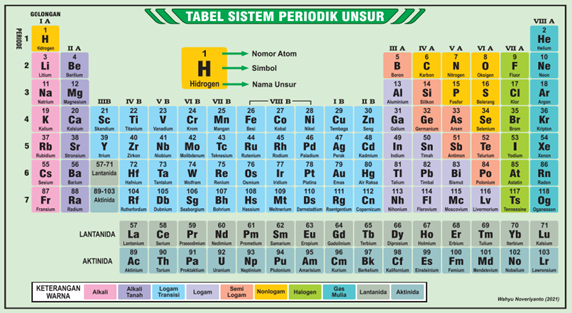
Dalam tabel periodik modern, atom dengan konfigurasi elektron yang serupa ditempatkan dalam satu kolom yang sama. Kolom ini dinamakan golongan yang dibaca dari atas ke bawah. Golongan menyatakan jumlah elektron kulit terluar (elektron valensi) suatu atom dari unsur tersebut. Sedangkan periode merupakan deretan unsur-unsur yang disusun berdasarkan peningkatan nomor atom berurutan dari kiri ke kanan. Periode mendeskripsikan jumlah kulit atom yang dimiliki oleh atom unsur tersebut.
Tabel periodik bentuk panjang terdiri dari 18 golongan dan 7 periode yang diuraikan sebagai berikut.
Bagian Horizontal
- Terdiri dari 7 baris horizontal disebut periode. Unsur-unsur pada periode disusun berdasarkan urutan nomor atom.
- Periode ke-1 adalah periode terpendek yaitu terdiri dari 2 unsur “H” dan “He”.
- Periode ke-2 dan ke-3 masing-masing memiliki 8 unsur.
- Periode ke-4 dan ke-5 masing-masing memiliki 18 unsur.
- Periode ke-6 memiliki 32 unsur.
Bagian Vertikal
- Kolom yang vertikal disebut golongan.
- Ada 18 golongan.
- Golongan dibagi menjadi 2 yaitu golongan utama (A) dan golongan transisi (B).
- Golongan utama terdiri dari golongan I A hingga VIII A (golongan 1 A hingga III A adalah unsur logam sedangkan golongan IV A hingga VIII A adalah nonlogam).
- Unsur B, Si, Ge, As, Sb, Te, Po, dan At adalah unsur-unsur semilogam atau metaloid.
- Golongan transisi terdiri dari golongan I B hingga VIII B yaitu unsurunsur logam transisi.
- Golongan lantanida dan aktinida juga dikelompokkan sebagai unsurunsur logam transisi.
Jari-jari Atom dalam Sistem Periodik Unsur

Bagaimana cara menghitung jari-jari atom? Pada gambar di bawah terdapat simbol “r” yaitu jari-jari dan “d” merupakan diameter. Adapun jari-jari atom dinyatakan dalam satuan Angstrom (Å). Satu Å = 100 pm (pikometer). Satu pm besarnya sama dengan 10–12 m. Ukuran jari-jari atom berkisar 30 - 300 pm.
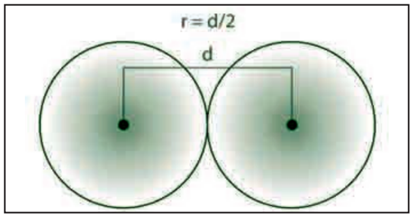
Jari-jari atom adalah jarak yang dihitung dari inti atom hingga lintasan paling luar suatu atom. Dalam satu golongan, jari-jari atom meningkat dari atas ke bawah. Adapun dalam satu periode, jari-jari atom meningkat dari kanan ke kiri. Dalam satu periode, semakin ke kanan jumlah proton dan neutron semakin banyak sehingga gaya tarik inti terhadap elektron terluar semakin kuat sehingga jari-jari atom semakin kecil.
Sifat jari-jari atom dalam sistem periodik unsur digambarkan dalam gambar berikut:
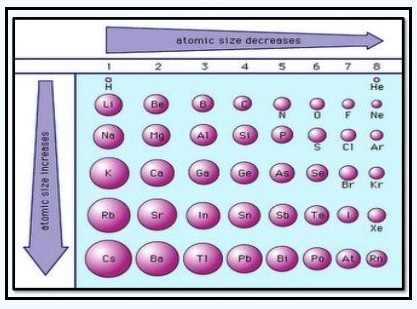
1.
Jawablah soal berikut ini!
Unsur yang terletak di sebelah kiri tabel periodik cenderung memiliki sifat....
A. Non-logam
B. Semikonduktor
C. Logam
D. Gas mulia
E. Metalurgi
JAWABAN BENAR
C.
Logam
PEMBAHASAN
Unsur yang terletak di sebelah kiri tabel periodik umumnya adalah logam, sedangkan non-logam cenderung terletak di sebelah kanan tabel periodik.
2.
Jawablah soal berikut ini!
Apakah yang menentukan letak unsur dalam golongan pada tabel periodik ?
A. Jumlah proton
B. Jumlah elektron valensi
C. Nomor atom
D. Jumlah elektron pada kulit terluar
E. Jumlah neutron
JAWABAN BENAR
B.
Jumlah elektron valensi
PEMBAHASAN
Golongan dalam tabel periodik ditentukan oleh jumlah elektron pada kulit terluar (elektron valensi) dari unsur tersebut.
3.
Jawablah soal berikut ini!
Golongan unsur yang memiliki sifat logam dan non-logam di tabel periodik disebut sebagai....
A. Golongan utama
B. Golongan transisi
C. Golongan logam
D. Golongan non-logam
E. Golongan lantanida
JAWABAN BENAR
A.
Golongan utama
PEMBAHASAN
Golongan unsur yang terletak di sebelah kiri dan kanan tengah tabel periodik, seperti Golongan IA (logam alkali), Golongan IIA (logam alkali tanah), Golongan IIIA-VIA, dan Golongan VIIA (halogen), merupakan golongan utama yang mencakup unsur dengan sifat logam dan non-logam.
4.
Jawablah soal berikut ini!
Jari-jari atom dapat diukur dalam satuan....
A. Nanometer (nm)
B. Meter (m)
C. Picometer (pm)
D. Kilometer (km)
E. Liter (L)
JAWABAN BENAR
C.
Picometer (pm)
PEMBAHASAN
Jari-jari atom umumnya diukur dalam satuan picometer (pm), di mana 1 pm setara dengan 1 x 10-12 meter.
5.
Jawablah soal berikut ini!
Pernyataan yang benar tentang jari-jari atom dalam satu periode pada tabel periodik adalah....
A. Jari-jari atom meningkat dari kiri ke kanan
B. Jari-jari atom berkurang dari kiri ke kanan.
C. Jari-jari atom tetap konstan dalam satu periode.
D. Tidak ada pola yang dapat dilihat dalam jari-jari atom dalam satu periode.
E. Semua jari-jari atom sama besarnya.
JAWABAN BENAR
B.
Jari-jari atom berkurang dari kiri ke kanan.
PEMBAHASAN
Jari-jari atom berkurang dari kiri ke kanan. Saat kita berpindah dari kiri ke kanan dalam satu periode, jumlah proton dalam inti atom bertambah, sehingga gaya tarik menarik terhadap elektron valensi juga meningkat. Hal ini mengakibatkan jari-jari atom yang lebih kecil.

Oops!!!
Yah, jawaban kamu meleset nih. Ingin melihat pembahasan soal ini?

BENAR!!!
Selamat!
Jawaban kamu benar. Ingin lihat pembahasan soal ini?
footer_v3
Bersama Aku Pintar temukan jurusan kuliah yang tepat
sesuai minat dan bakatmu.
Aku Pintar memiliki visi membuat pendidikan merata, mudah dijangkau, dan terjangkau dengan Program Journey Pintar yang merupakan sebuah program persiapan lengkap bagi siswa SMA/SMK/sederajat yang ingin masuk ke perguruan tinggi impiannya.
Kontak Kami
Grand Slipi Tower Lt. 42
Jl. S. Parman Kav 22-24
Jakarta Barat
© 2024 Aku Pintar. All Rights Reserved

