Belajar Pintar Materi SMP, SMA, SMK
BelajarPintarV3
Kimia
Ikatan Kimia
MATERI
Pengertian Ikatan Kimia

Kita semua tahu bahwa manusia merupakan makhluk sosial yang membutuhkan manusia lainnya untuk saling membantu satu sama lain dengan begitu manusia juga membentuk ikatan antar manusia lainnya seperti, ikatan teman, ikatan keluarga, ikatan saudara, dan juga ikatan cinta.
Sama halnya dengan manusia, setiap unsur dalam bentuk atom juga dapat membentuk suatu ikatan dengan atom yang lainnya dengan adanya suatu ikatan kimia.
Ikatan kimia adalah ikatan antara atom-atom untuk membentuk senyawa, sehingga mencapai kestabilan. Secara umum, ikatan kimia yang kuat diasosiasikan dengan transfer elektron antara dua atom yang berpartisipasi. Ikatan kimia menjaga molekul-molekul, kristal, dan gas-gas diatomik untuk tetap bersama. Selain itu ikatan kimia juga menentukan struktur dan sifat suatu zat.
Macam-macam ikatan kimia diantaranya:
- Ikatan ion
- Ikatan kovalen
- Ikatan logam
Selain itu, antar molekul yang berdekatan juga dapat mengalami suatu gaya tarik menarik, macam-macam gaya antar molekul tersebut adalah sebagai berikut:
- Gaya London
- Gaya dipol-dipol
- Gaya Van der Waals
- Ikatan hidrogen
Kestabilan Atom

Untuk mencapai keadaan stabil, suatu atom akan mengalami ikatan kimia. Elektron valensi sangat berperan dalam mengadakan ikatan kimia.
Suatu atom disebut stabil jika mempunyai konfigurasi elektron mirip gas mulia yaitu pada kulit terakhir mempunyai 8 elektron (oktet) atau 2 elektron (duplet jika jumlah kulit hanya 1). Namun, kadang-kadang terjadi penyimpangan oktet, dimana elektron valensi jumlahnya lebih dari 8, namun atom tetap stabil.
Untuk mencapai kestabilan, atom yang berikatan akan mengalami:
- Serah terima elektron (pelepasan dan penerimaan elektron)
- Penggunaan pasangan elektron bersama
Berikut ini adalah tabel unsur gas mulia:
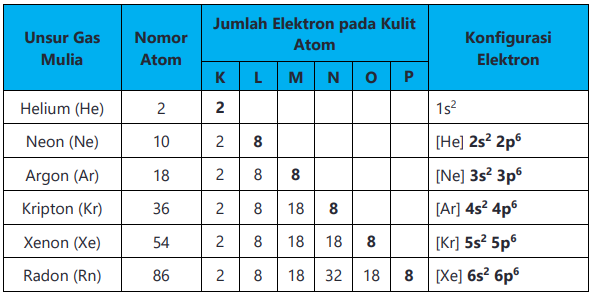
1.
Kerjakan soal berikut ini dengan tepat!
Untuk mencapai kestabilan suatu atom harus memiliki elektron valensi seperti...
A. alkali
B. alkali tanah
C. gas mulia
D. logam mulia
E. logam berat
JAWABAN BENAR
C.
gas mulia
PEMBAHASAN
Untuk mencapai kestabilan suatu atom jumlah elektron valensinya harus mencapai seperti yang dimiliki oleh gas mulia
2.
Kerjakan soal berikut ini dengan tepat!
Susunan elektron valensi gas mulia dibawah ini yang tidak oktet adalah....
A. Xe
B. Kr
C. Ar
D. Ne
E. He
JAWABAN BENAR
E.
He
PEMBAHASAN
Dari beberapa unsur gas mulia, hanya helium yang memiliki kestabilan pada 2 elektron valensi atau duplet.
3.
Kerjakan soal berikut ini dengan tepat!
Kestabilan gas mulia dijadikan pijakan atom-atom lain, sehingga atom-atom tersebut menginginkan konfigurasi seperti gas mulia dengan melakukan cara cara dibawah ini, kecuali ....
A. Pelepasan elektron
B. Penyerapan elektron
C. Memasangkan elektron
D. Menerima pasangan elektron
E. Menerima minimal dua pasang elektron
JAWABAN BENAR
E.
Menerima minimal dua pasang elektron
PEMBAHASAN
Kestabilan atom dapat diperoleh dengan melepas, penerima, memasangkan, menerima pasangan elektron, atau meminjamkan pasangan elektron.
4.
Kerjakan soal berikut ini dengan tepat!
Diantara unsur unsur di bawah ini yang paling stabil adalah ....
A. 8P
B. 9Q
C. 10R
D. 12S
E. 20T
JAWABAN BENAR
C.
10R
PEMBAHASAN
10R merupakan unsur yang paling stabil karena memiliki elektron valensi berjumlah 8:
10R : 2, 8
5.
Kerjakan soal berikut ini dengan tepat!
Suatu unsur konfigurasi elektronnya adalah 2 6. Kecenderungan unsur tersebut bila akan berikatan dengan unsur yang lain adalah ....
A. Melepas 2 elektron sehingga bermuatan +2
B. Melepas 4 elektron sehingga bermuatan +4
C. Menyerap 2 elektron sehingga bermuatan –2
D. Menyerap 4 elektron sehingga bermuatan –4
E. Memasangkan keempat elektronnya dengan 4 elektron lain
JAWABAN BENAR
C.
Menyerap 2 elektron sehingga bermuatan –2
PEMBAHASAN
Karena jumlah elektron valensinya 6 untuk mencapai kestabilannya lebih cenderung untuk menyerap elektron sehingga bermuatan -2.
6.
Kerjakan soal berikut ini dengan tepat!
Unsur Al dengan nomor atom 13 mempunyai konfigurasi elektron 1s2 2s2 2p6 3s2 3p1. Konfigurasi elektron yang tepat untuk ion Al agar memenuhi kaidah oktet adalah ....
A. 1s2 2s2 2p6 3s2 3p6
B. 1s2 2s2 2p6 3s2 3p1
C. 1s2 2s2 2p6 3p1
D. 1s2 2s2 2p6 3s2
E. 1s2 2s2 2p6
JAWABAN BENAR
E.
1s2 2s2 2p6
PEMBAHASAN
Elektron terluar unsur Al berjumlah 3 pada kulit ke 3, sehingga melepaskan 3 elektron untuk memenuhi kaidah oktet.
13Al = 1s2 2s2 2p6 3s2 3p1
13Al3+ = 1s2 2s2 2p6
7.
Kerjakan soal berikut ini dengan tepat!
Atom-atom berikut dapat memenuhi kaidah oktet dengan melepaskan atau menerima elektron, kecuali ....
A. 19K
B. 13Al
C. 8O
D. 7N
E. 3Li
JAWABAN BENAR
E.
3Li
PEMBAHASAN
3Li = [He] 2s1
3Li+ = [He]
Atom Li memenuhi kaidah duplet.

Oops!!!
Yah, jawaban kamu meleset nih. Ingin melihat pembahasan soal ini?

BENAR!!!
Selamat!
Jawaban kamu benar. Ingin lihat pembahasan soal ini?
footer_v3
Bersama Aku Pintar temukan jurusan kuliah yang tepat
sesuai minat dan bakatmu.
Aku Pintar memiliki visi membuat pendidikan merata, mudah dijangkau, dan terjangkau dengan Program Journey Pintar yang merupakan sebuah program persiapan lengkap bagi siswa SMA/SMK/sederajat yang ingin masuk ke perguruan tinggi impiannya.
Kontak Kami
Grand Slipi Tower Lt. 42
Jl. S. Parman Kav 22-24
Jakarta Barat
© 2024 Aku Pintar. All Rights Reserved

