Materi Kimia - Larutan Elektrolit dan Non Elektrolit Kelas 10 MIA - Belajar Pintar
BelajarPintarV3
Peta Belajar Bersama
Sobat, ini nih, ada Peta Belajar Bersama Kimia di bab keempat.
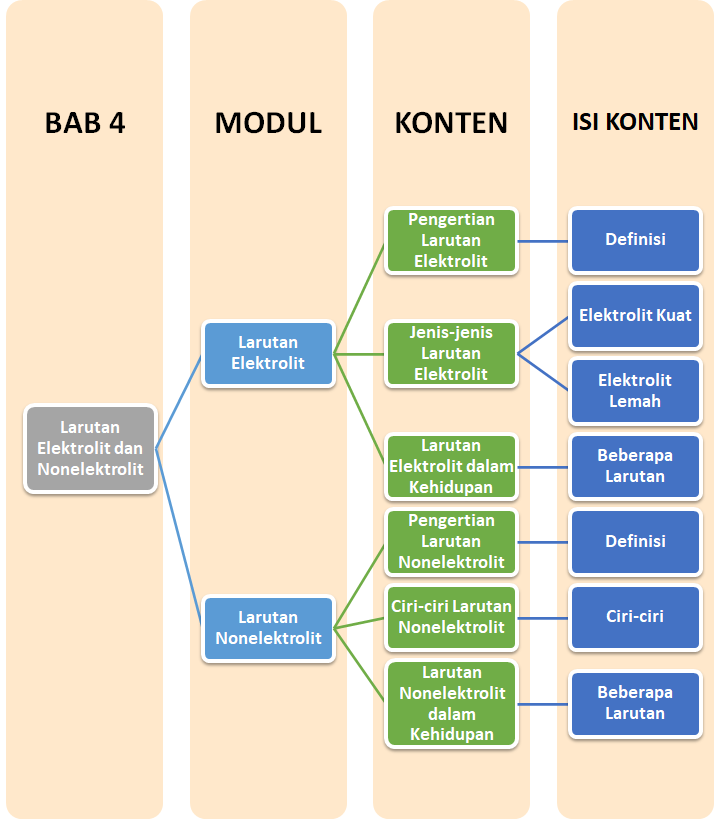
Yuk, mulai belajar bersama!
Pengertian Larutan Elektrolit

Larutan elektrolit adalah larutan yang dapat menghantarkan arus listrik. Dalam larutan elektrolit molekul-molekulnya terurai (terdisosiasi) menjadi partikel-partikel bermuatan listrik positif dan negatif yang disebut ion (ion positif-ion negatif). Ion positif yang dihasilkan dinamakan kation dan ion negatif yang dihasilkan dinamakan anion.
Larutan elektrolit dapat menghantarkan listrik karena:
- Pada senyawa ionik, larutan terion menjadi ion-ion bermuatan listrik yang bergerak bebas menghantarkan listrik.
Contoh: NaCl --> Na+ + Cl-
Dapat menghantarkan listrik dalam bentuk larutan dan lelehan. - Pada senyawa kovalen polar, larutan terion akibat gaya tarik antar molekul yang memutuskan ikatan atom molekul.
Contoh: CH3COOH --> CH3COO- + H+
Dapat menghantarkan listrik dalam bentuk larutan. Lelehannya tidak dapat menghantarkan listrik.
Pengertian Larutan Nonelektrolit

Larutan non-elektrolit adalah larutan yang tidak dapat menghantarkan arus listrik. Larutan-larutan non-elektrolit terdiri atas zat-zat yang terlarut dalam air namun tidak terurai menjadi ion (tidak terionisasi). Dalam larutan, zat non-elektrolit tetap seperti molekul yang tidak bermuatan listrik. Itulah mengapa larutan ini tidak dapat menghantarkan arus listrik.
Ketika dilarutkan ke dalam air, larutan-larutan nonelektrolit seperti larutan gula dan alkohol tidak terurai menjadi ion-ionnya. Larutan nonelektrolit terurai menjadi molekul-molekulnya. Larutan gula dan larutan alkohol termasuk senyawa kovalen nonpolar. Berdasarkan hal tersebut dapat disimpulkan bahwa senyawa kovalen nonpolar merupakan senyawa nonelektrolit.
Contoh larutan non-elektrolit adalah Larutan urea, larutan sukrosa, larutan glukosa, dan larutan alkohol
Materi Kimia SMA - 10 MIA Lainnya
footer_v3
Bersama Aku Pintar temukan jurusan kuliah yang tepat
sesuai minat dan bakatmu.
Aku Pintar memiliki visi membuat pendidikan merata, mudah dijangkau, dan terjangkau dengan Program Journey Pintar yang merupakan sebuah program persiapan lengkap bagi siswa SMA/SMK/sederajat yang ingin masuk ke perguruan tinggi impiannya.
Kontak Kami
Grand Slipi Tower Lt. 42
Jl. S. Parman Kav 22-24
Jakarta Barat
© 2024 Aku Pintar. All Rights Reserved