Materi Kimia - Senyawa Karbon Turunan Alkana Kelas 12 MIA - Belajar Pintar
BelajarPintarV3
Peta Belajar Bersama
Sobat, ini nih, ada Peta Belajar Bersama Kimia di bab keempat.
Yuk, mulai belajar bersama!
Pengertian Gugus Fungsi

Di kelas XI telah kita pelajari senyawa karbon, yaitu golongan hidrokarbon yang terdiri atas alkana, alkena, dan alkuna. Senyawa karbon yang akan kita pelajari pada bagian ini merupakan turunan dari alkana. Bila satu atau lebih atom H pada alkana diganti dengan atom atau gugus lain akan dihasilkan senyawa turunan alkana.
Perhatikan struktur metana dan metanol berikut:
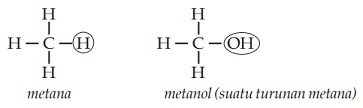
Gugus –OH pada metanol menggantikan atom H pada metana. Gugus pengganti ini disebut gugus fungsi. Suatu senyawa yang memiliki rumus molekul sama dapat memiliki rumus struktur yang berbeda. Disebut apakah peristiwa ini?
Senyawa dengan rumus molekul C2H6O dapat berupa etanol dan metoksi metana.
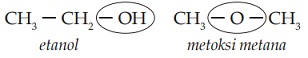
Kedua senyawa tersebut memiliki sifat yang berbeda, mengapa?
Etanol dan metoksi metana memiliki gugus fungsi yang berbeda, yaitu OH dan O. Hal ini menunjukkan bahwa sifat suatu senyawa karbon ditentukan oleh gugus fungsinya. Gugus fungsi adalah atom atau gugus yang menentukan sifat suatu senyawa.
Pengertian, Tata Nama, dan Jenis Alkohol

Alkohol yang dikenal dalam kehidupan sehari-hari adalah etanol yang merupakan salah satu anggota deret homolog alkohol. Alkohol merupakan golongan senyawa dengan rumus umum R-OH, di mana R adalah alkil (R = CnH2n+1). Dengan demikian alkohol dapat dianggap sebagai turunan dari alkana (R-H) di mana 1 atom H nya diganti dengan gugus -OH.
Tata Nama Alkohol/Alkanol
Oleh karena alkohol dianggap sebagai turunan dari alkana, maka alkohol diberi nama seperti alkana, hanya akhiran ana diganti dengan akhiran anol.
Contoh:
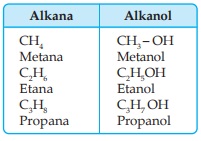
Alkanol yang sudah berisomer, diberi nama dengan cara:
Menyebutkan nomor atom C terlebih dahulu yang mengikat OH kemudian nama alkanol (pengertian nomor dimulai dari atom C yang dekat dengan -OH)
Contoh:
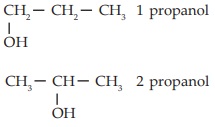
Alkohol yang bercabang diberi nama dengan cara:
Menyebutkan nomor cabang, nama cabang, letak OH, dan nama alkanol rantai utama (atom C yang mengikat OH diberi nomor serendah mungkin)
Contoh:
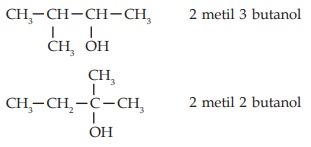
Jenis-Jenis Alkohol
Berdasarkan letak gugus -OH, alkohol dibedakan menjadi 3 macam, yaitu:
- Alkohol Primer
Alkohol primer adalah alkohol yang gugus-OH nya terikat pada atom C primer (atom C yang terikat pada satu atom C lain).
Contoh: CH3-CH2-OH dan CH3-CH2-CH2-OH - Alkohol Sekunder
Alkohol sekunder adalah alkohol yang gugus-OH nya terikat pada atom C sekunder.
Contoh:
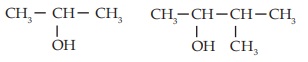
- Alkohol Tersier
Alkohol tersier adalah alkohol yang gugus -OH nya terikat pada atom C tersier.
Contoh:
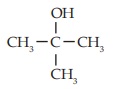
Pengertian, Tata Nama, dan Isomer Eter

Sebagaimana telah disebutkan di modul sebelumnya, eter merupakan isomer fungsi dari alkohol. Eter memiliki rumus umum R-O-R, dengan R adalah alkil. Alkil-alkil pada eter dapat disamakan dan dapat pula dibedakan.
Tata Nama Eter atau Alkoksi Alkana
- Sebagai Eter
Dengan cara menyebutkan nama alkil-alkilnya (sesuai urutan abjad) dan diakhiri dengan kata eter.
Contoh:
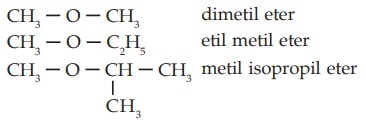
- Sebagai Alkoksi Alkana
Dengan cara menyebutkan nama alkoksinya (dari R/alkil yang lebih kecil) yang diawali nomor letak gugus alkoksi kemudian nama alkananya (dari R/alkil yang lebih besar).
Contoh:
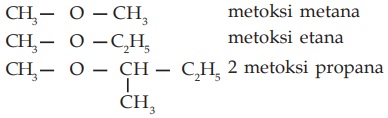
Isomer Eter
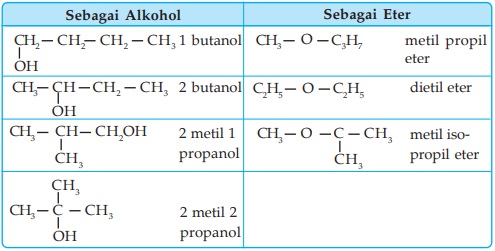
Eter selain berisomer dengan sesamanya, juga berisomer dengan alkohol (isomer fungsi) yang rumusnya sama yaitu CnH2n+2O.
Contoh: isomer C4H10O
Pengertian, Tata Nama, dan Isomer Aldehid

Aldehid atau alkanal dapat dianggap sebagai turunan alkana dengan mengganti -CH3 dari alkana dengan gugus fungsi -CHO.
Rumus umum aldehid adalah R-CHO , dengan R adalah alkil.
Tata Nama Aldehid atau Alkanal
Aldehid dapat diberi nama dengan dua cara, yaitu:
- Nama sebagai alkanal (nama IUPAC).
Nama alkanal seperti alkana dengan mengganti akhiran ana dengan -anal serta nomor 1 dimulai dari gugus -CHO
Contoh:
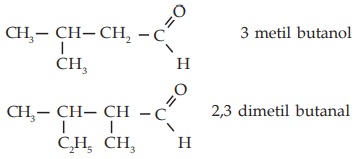
- Nama sebagai Aldehid (nama trivial)
Beberapa nama aldehid adalah sebagai berikut:
H-CHO = metanal = formaldehid
CH3-CHO = etanal = asetaldehid
CH3-CH2-CHO = propanal = propionaldehid
Isomer Alkanal
Isomer alkanal disebabkan oleh adanya cabang dan letak cabang.
Contoh : isomer butanal (C4H8O)
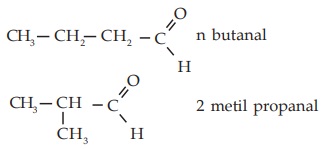
Pengertian, Tata Nama, dan Isomer Alkanon

Alkanon merupakan isomer fungsi dari aldehid dengan gugus fungsional -CO-. Rumus umum alkanon adalah R-CO-R dengan R adalah alkil.
Tata Nama Alkanon
- Sistem IUPAC, seperti pada alkana, hanya akhiran ana diganti dengan anon.
Contoh:
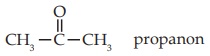
- Sistem trivial (sebagai keton)
Dengan menyebutkan alkil-alkil yang mengapit gugus sesuai urutan abjad dan diakhiri dengan keton.
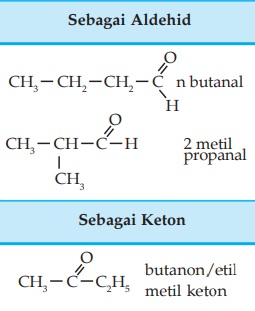
Contoh:
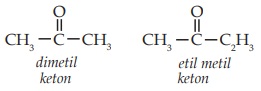
Isomer Alkanon
Isomer alkanon disebabkan oleh cabang, letak gugus fungsional, dan isomer fungsional dengan aldehid.
Contoh: isomer C4H8O
Pengertian, Tata Nama, dan Isomer Asam Karboksilat

Asam karboksilat atau alkanoat dapat dianggap turunan alkana yang memiliki gugus -COOH. Rumus umum asam karboksilat adalah R-COOH dengan R adalah alkil.
Tata Nama Asam Karboksilat
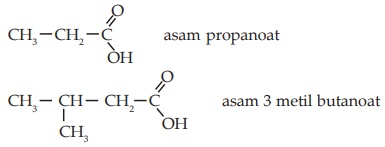
Nama asam karboksilat diturunkan dari nama alkana dengan menggantikan akhiran ana dengan anoat dan penomoran dimulai dari gugus fungsi -COOH terlebih dahulu serta penambahan awalan asam.
Contoh:
Isomer Asam Karboksilat
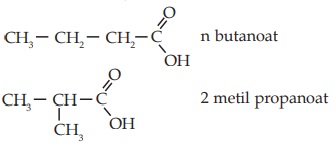
Isomer asam karboksilat disebabkan ada tidaknya cabang dan letak cabang, selain itu asam karboksilat juga berisomer fungsi dengan ester.
Contoh: isomer C3H7COOH
Pengertian, Tata Nama, dan Isomer Ester

Ester merupakan isomer fungsi dari asam karboksilat dengan gugus fungsi -COO-. Rumus umum asam ester adalah R-COO-R dengan R adalah alkil.
Tata Nama
Ester Dengan menyebutkan gugus alkilnya, kemudian diikuti karboksilatnya.
Contoh:
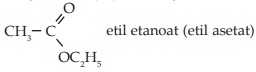
Isomer Ester
Isomer ester disebabkan oleh gugus alkil dan gugus alkanoatnya. Selain itu ester juga berisomer dengan asam karboksilat.
Contoh: isomer C4H8O2
- Sebagai asam karboksilat
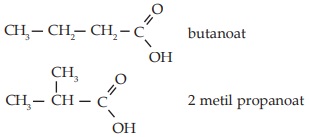
- Sebagai ester
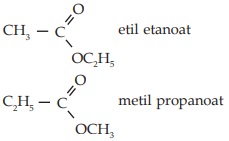
Pengertian dan Tata Nama Haloalkana

Haloalkana adalah senyawa-senyawa yang dapat dianggap berasal dari alkana, di mana satu atau lebih atom H diganti dengan atom halogen. Rumus umum haloalkana adalah R-X dengan X adalah alkil (R = CnH2n+1) dan X adalah atom halogen (X = F, Cl, Br, atau I).
Contoh:
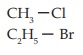
Tata Nama Haloalkana
- Haloalkana diberi nama dengan menyebut nama halogen yang terikat (Fluoro, kloro, bromo, iodo) yang diikuti nama alkananya.
Contoh:
CH3-Cl kloro metana
CH3-CH2-Br bromo etana
CCl4 tetra kloro metana
Haloalkana yang telah memiliki isomer diberi nama dengan menyebut nomor yang menyatakan letak halogen (pemberian nomor dimulai dari ujung yang dekat dengan halogen sehingga nomor letak halogen sekecil mungkin). Aturan lain seperti pada alkana.
Contoh:
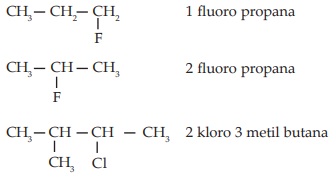
footer_v3
Bersama Aku Pintar temukan jurusan kuliah yang tepat
sesuai minat dan bakatmu.
Aku Pintar memiliki visi membuat pendidikan merata, mudah dijangkau, dan terjangkau dengan Program Journey Pintar yang merupakan sebuah program persiapan lengkap bagi siswa SMA/SMK/sederajat yang ingin masuk ke perguruan tinggi impiannya.
Kontak Kami
Grand Slipi Tower Lt. 42
Jl. S. Parman Kav 22-24
Jakarta Barat
© 2024 Aku Pintar. All Rights Reserved