Materi Kimia - Kesetimbangan Kimia Kelas 11 MIA - Belajar Pintar
BelajarPintarV3
Peta Belajar Bersama
Sobat, ini nih, ada Peta Belajar Bersama Kimia di bab keempat.
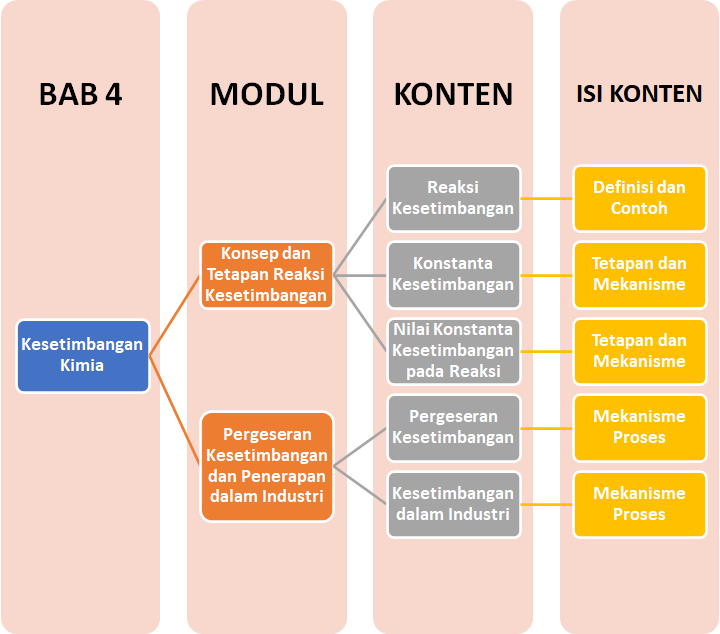
Yuk, mulai belajar bersama!
Reaksi Kesetimbangan

Reaksi Kimia (Reversible dan Irreversible)
Berdasarkan arahnya, reaksi dapat dibedakan menjadi reaksi berkesudahan (irreversible/satu arah) dan reaksi bolak balik (reversibel/dua arah).
Pada reaksi berkesudahan, hasil reaksi tidak dapat diubah lagi menjadi zat pereaksi. Misalnya, pada reaksi pembakaran kayu atau proses pengkaratan besi. Abu atau arang hasil pembakaran tidak dapat diubah kembali menjadi kayu seperti semula.
Di lain pihak, ada reaksi bolak balik, yaitu reaksi yang berlangsung dalam dua arah dimana zat-zat hasil reaksi dapat bereaksi kembali membentuk zat pereaksi. Sebagai contoh, reaksi antara timbal (II) sulfat dengan natrium iodida.
- Jika serbuk timbal (II) sulfat direaksikan dengan larutan natrium iodida, terbentuk endapan kuning dari timbal (II) iodida:
PbSO4(s) + 2NaI(aq) ---> PbI2(s) + Na2SO4(aq) - Sebaliknya, bila endapan timbal (II) iodida direaksikan dengan larutan natrium sulfat, maka akan terbentuk kembali endapan timbal (II) sulfat yang berwarna putih:
PbI2(s) + Na2SO4(aq) ---> PbSO4(s) + 2NaI(aq) - Kedua reaksi tersebut dapat digabungkan sebagai berikut :
PbSO4(s) + 2NaI(aq) <==> PbI2(s) + Na2SO4(aq)
Penulisan reaksi bolak balik ditandai dengan dua panah yang arahnya berlawanan.
Dengan demikian, pada reaksi tersebut terjadi proses kesetimbangan dinamis, yaitu proses bolak balik yang lajunya sama untuk kedua arah.
Kesetimbangan Kimia
Ciri-ciri Kesetimbangan Kimia:
- Reaksi berlangsung dua arah dan dalam ruang tertutup.
- Laju reaksi ke kiri = laju reaksi ke kanan.
- Tidak terjadi perubahan makroskopis, tetapi terjadi perubahan mikroskopis.
Perhatikan grafik kesetimbangan berikut ini:
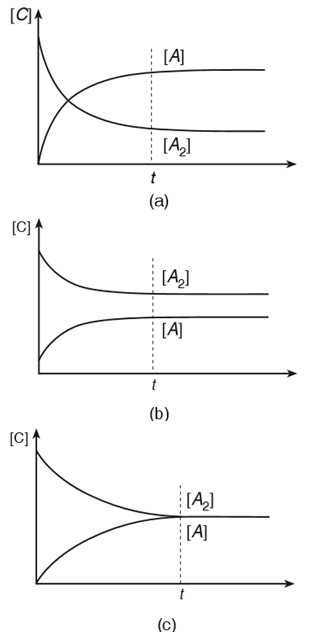
- Grafik (a), Pada saat setimbang konsentrasi produk ([A]) lebih besar daripada konsentrasi reaktan ([A2]).
- Grafik (b), Pada saat setimbang konsentrasi produk ([A]) lebih kecil daripada konsentrasi reaktan ([A2]).
- Grafik (c), Pada saat setimbang konsentrasi produk ([A]) sama dengan konsentrasi reaktan ([A2]).
Reaksi Kesetimbangan Homogen dan Heterogen
- Reaksi Kesetimbangan Homogen
Reaksi kesetimbangan homogen merupakan reaksi kesetimbangan dengan komponen berfase sama dapat berupa sistem gas atau larutan.
Contoh kesetimbangan reaksi homogen dengan komponen reaksinya gas:
N2(g) + 3H2(g) <==> 2NH3(g)
Semua komponen baik reaktan maupun produk reaksi adalah berfase gas - Reaksi Kesetimbangan Heterogen
Reaksi kesetimbangan heterogen merupakan reaksi dengan komponen reaksinya terdiri dari fase yang berbeda dapat dua atau lebih fase yang berbeda
Contoh kesetimbangan reaksi heterogen adalah sebagai berikut:
CaCO3(s) <==> CaO(s) + CO2(g)
Reaksi tersebut terdiri dari dua fase, yaitu padatan dan gas. Reaktan terdiri dari senyawa yang berfase padat, sedangkan produk terdiri dari senyawa padat, yaitu CaO dan fase gas, yaitu CO2
Pergeseran Kesetimbangan

Azas Le Chatelier menjelaskan bagaimana terjadinya pergeseran kesetimbangan. "Bila suatu kesetimbangan diberikan suatu aksi/tindakan, maka sistem tersebut akan mengadakan reaksi yang cenderung mengurangi aksi tersebut".
Pergeseran kesetimbangan tidak mengubah nilai Kc dan Kp, kecuali suhu pada sistem kesetimbangan berubah.
Konsep pergeseran kesetimbangan:
- Kesetimbangan dikatakan bergeser ke kiri apabila zat di kiri bertambah atau zat di kanan berkurang.
- Kesetimbangan dikatakan bergeser ke kanan apabila zat di kanan bertambah atau zat di kiri berkurang.
Berikut merupakan faktor-faktor yang mempengaruhi pergeseran kesetimbangan:
Pengaruh Konsentrasi
- Jika konsentrasi diperbesar pada reaktan atau produk, kesetimbangan akan bergerak ke arah sisi (reaktan atau produk) yang konsentrasinya tidak diperbesar.
- Jika konsentrasi diperkecil pada reaktan atau produk, kesetimbangan akan bergerak ke arah sisi (reaktan atau produk) yang konsentrasinya diperkecil.
Pengaruh Tekanan
- Jika tekanan diperbesar (volume diperkecil), kesetimbangan akan bergerak ke arah yang jumlah koefisiennya terkecil.
- Jika tekanan diperkecil (volume diperbesar), kesetimbangan akan bergerak ke arah yang jumlah koefisiennya terbesar.
Pengaruh Suhu
- Jika suhu dinaikkan, kesetimbangan akan bergeser ke arah reaksi endoterm.
- Jika suhu diturunkan, kesetimbangan akan bergeser ke arah reaksi eksoterm.
Pengaruh Katalis
Katalis dapat mempercepat pencapaian keadaan setimbang, namun katalis tidak mengubah komposisi kesetimbangan.
Materi Kimia SMA - 11 MIA Lainnya
footer_v3
Bersama Aku Pintar temukan jurusan kuliah yang tepat
sesuai minat dan bakatmu.
Aku Pintar memiliki visi membuat pendidikan merata, mudah dijangkau, dan terjangkau dengan Program Journey Pintar yang merupakan sebuah program persiapan lengkap bagi siswa SMA/SMK/sederajat yang ingin masuk ke perguruan tinggi impiannya.
Kontak Kami
Grand Slipi Tower Lt. 42
Jl. S. Parman Kav 22-24
Jakarta Barat
© 2024 Aku Pintar. All Rights Reserved