Materi Kimia - Koloid Kelas 11 MIA - Belajar Pintar
BelajarPintarV3
Peta Belajar Bersama
Sobat, ini nih, ada Peta Belajar Bersama Kimia di bab kesembilan.
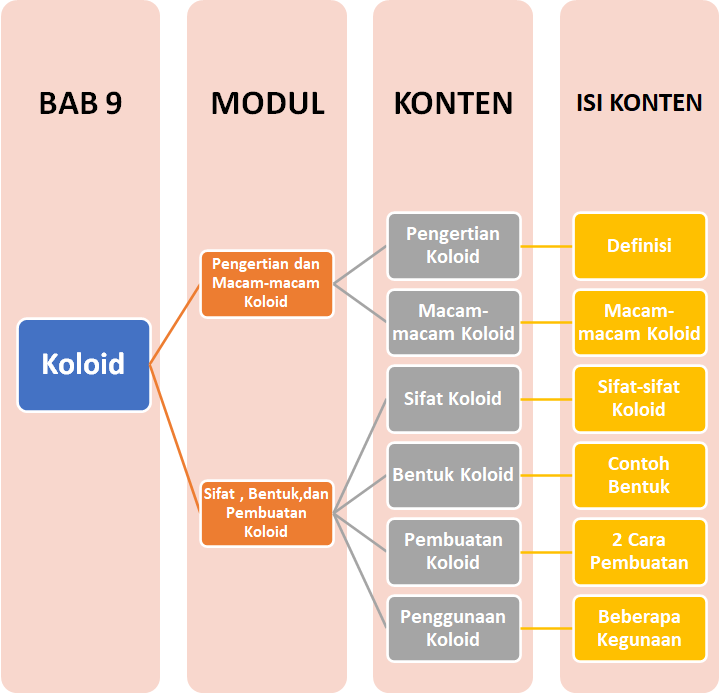
Yuk, kita belajar bersama!
Pengertian Koloid

Koloid adalah suatu bentuk campuran yang keadaannya antara larutan dan suspensi. Atau dapat juga diartikan sebagai suatu sistem dispersi yang ukuran partikelnya lebih besar dari larutan, tetapi lebih kecil dari suspensi (campuran kasar).
Koloid tergolong sistem dua fase, yaitu:
- Fase terdispersi (terlarut), adalah zat yang didispersikan, bersifat diskontinu (terputus-putus).
- Medium dispersi (pelarut), adalah zat yang menjadi medium untuk dispersi, bersifat kontinu (berkelanjutan).
Koloid tergolong campuran heterogen walau tampak homogen secara makroskopis, karena perbedaan partikel kedua fase masih dapat diamati secara mikroskopis.
Ciri-ciri sistem larutan:
- Dispersi molekuler.
- Sifat campuran homogen.
- Dimensi partikel kurang dari 1 nm.
- Sistem satu fase dan relatif stabil.
- Tidak dapat disaring.
Contoh: larutan gula, larutan garam, alkohol, cuka, spirtus, air laut, bensin, udara bersih.
Ciri-ciri sistem suspensi:
- Dispersi kasar.
- Sifat campuran heterogen.
- Dimensi partikel lebih dari 100 nm.
- Sistem dua fase dan tidak stabil.
- Dapat disaring.
Contoh: air keruh, air berpasir, kopi, air + minyak.
Ciri-ciri sistem koloid:
- Dispersi koloid.
- Sifat campuran homogen secara makroskopis, namun heterogen secara mikroskopis.
- Dimensi partikel antara 1 – 100 nm.
- Sistem dua fase dan relatif stabil.
- Tidak dapat disaring, kecuali menggunakan penyaring ultra.
Contoh: tinta, cat, darah, sabun, asap, jelly, susu, santan, awan, kabut, busa, krim kocok, sitoplasma.
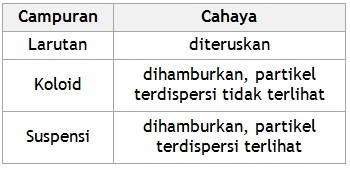
Perbedaan Larutan, Koloid, dan Suspensi
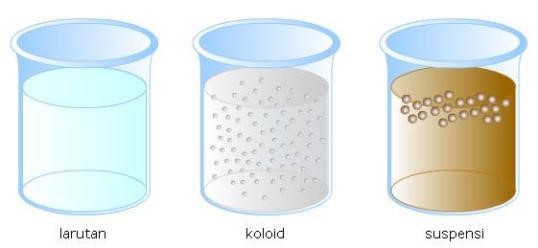
Sifat Koloid

Sifat-sifat koloid antara lain:
Efek Tyndall
Efek Tyndall adalah efek penghamburan cahaya oleh partikel koloid.
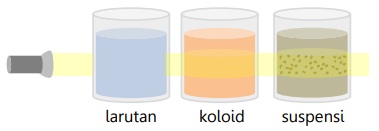
Contoh efek Tyndall:
- Sorot lampu mobil ketika berkabut.
- Sorot lampu proyektor film dalam bioskop yang diberi asap.
- Berkas sinar matahari melalui celah daun pohon di pagi yang berkabut.
Gerak Brown
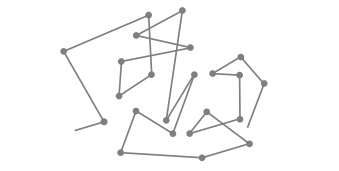
Gerak Brown adalah gerak acak zig-zag partikel koloid yang disebabkan oleh tumbukan tak setimbang antara partikel terdispersi dengan pendispersi.
Gerak Brown menstabilkan koloid karena mengimbangi gaya gravitasi yang dapat menyebabkan pengendapan.
Muatan koloid
Muatan koloid terbentuk karena koloid dapat mengalami adsorpsi, elektroforesis dan koagulasi.
Muatan koloid menstabilkan koloid karena partikel-partikel koloid bermuatan sama sehingga saling tolak-menolak, sehingga menghindari penggumpalan.
Adsorpsi (penyerapan pada permukaan)
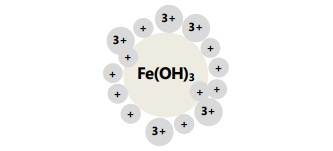
Adsorpsi adalah sifat partikel koloid yang dapat menyerap ion atau molekul netral pada permukaannya.
- Koloid positif mengadsorpsi kation.
Contoh: sol Fe(OH)3, sol Al(OH)3, pigmen pewarna, hemoglobin. - Koloid negatif mengadsorpsi anion.
Contoh: sol emas, sol perak, sol fosfor, sol As2S3, tepung, tanah liat.
Contoh adsorpsi:
- Sol Fe(OH)3 bermuatan positif dan mengadsorpsi ion H+ dan Fe3+.
- Sol As2S3 bermuatan negatif dan mengadsorpsi ion S2-.
- Sol AgCl bermuatan positif bila mengadsorpsi ion Ag+, bermuatan negatif bila mengadsorpsi ion Cl-.
Elektroforesis
Elektroforesis adalah sifat partikel koloid yang dapat bergerak dalam medan listrik.
Muatan koloid dapat ditentukan dengan memberi medan listrik di sekitar koloid.
- Koloid positif akan bergerak ke katoda atau elektroda negatif.
- Koloid negatif akan bergerak ke anoda atau elektroda positif.
Koagulasi
Koagulasi adalah penggumpalan koloid akibat hilangnya muatan koloid.
Koagulasi kimiawi dapat terjadi akibat:
- Percampuran koloid beda muatan
Menyebabkan koloid saling menetralkan satu sama lain dan menggumpal. - Penambahan elektrolit
Elektrolit dapat menetralkan koloid dan menyebabkan koagulasi.
Koagulasi terjadi bila koloid positif ditambah elektrolit yang lebih negatif, dan koloid negatif ditambah elektrolit yang lebih positif. - Elektroforesis
Terjadi ketika koloid mencapai elektroda.
Contoh koagulasi:
- Delta terbentuk akibat tanah liat terkoagulasi ketika bercampur dengan air laut.
- Asap pabrik digumpalkan dengan alat koagulasi listrik Cottrel.
Materi Kimia SMA - 11 MIA Lainnya

Hidrokarbon dan Minyak Bumi
6 Sub Bab Materi

Hukum Termokimia
4 Sub Bab Materi

Laju Reaksi
4 Sub Bab Materi

Kesetimbangan Kimia
3 Sub Bab Materi

Larutan Asam dan Basa
4 Sub Bab Materi

Hidrolisis Garam
3 Sub Bab Materi

Larutan Penyangga
2 Sub Bab Materi

Kelarutan dan Hasil Kali Kelarutan
3 Sub Bab Materi
footer_v3
Bersama Aku Pintar temukan jurusan kuliah yang tepat
sesuai minat dan bakatmu.
Aku Pintar memiliki visi membuat pendidikan merata, mudah dijangkau, dan terjangkau dengan Program Journey Pintar yang merupakan sebuah program persiapan lengkap bagi siswa SMA/SMK/sederajat yang ingin masuk ke perguruan tinggi impiannya.
Kontak Kami
Grand Slipi Tower Lt. 42
Jl. S. Parman Kav 22-24
Jakarta Barat
© 2024 Aku Pintar. All Rights Reserved